미래창조과학부는 서울대 약학대학 이호영 교수(사진) 연구팀이 ‘표적 항암제’의 새로운 내성 생성 및 작용 원리를 발견해 내성으로 인한 암 재발을 억제할 수 있는 새로운 항암 치료 전략을 제시했다고 28일 밝혔다.
‘표적 항암제’는 암 생성 때 생기는 생체물질의 활동을 억제해서 증식을 막고 사멸을 유도하는 항암제다. 정상세포까지 공격하는 기존 항암제와는 달리 암세포가 증식하는 데 필요한 요소들의 활동만 선택적으로 차단ㆍ억제하기 때문에 부작용이 적어 최근 활발히 개발되고 있다.
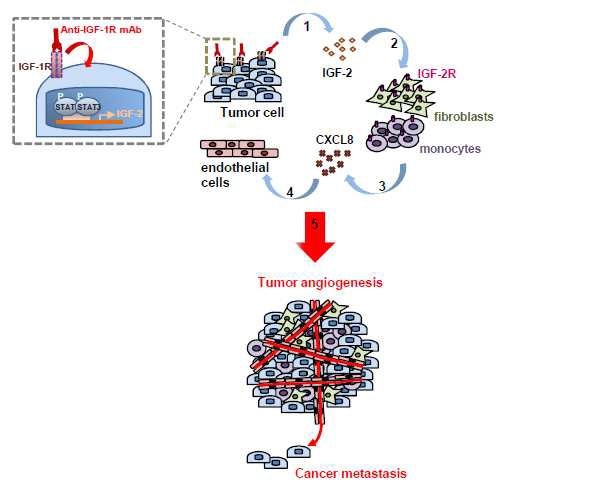 |
| 서울대 약학대 이호영 교수팀이 밝혀낸 표적항암제의 내성 및 전이암 기전 규명 연구 모식도. IGF-1R 표적 항암제에 의하여 IGF2가 생성되고 이를 인식해 종양 주변 세포들인 섬유아세포와 단핵세포가 이동하면 혈관 생성을 촉진하는 물질(사이토카인인 CXCL8)이 분비돼 전이암 생성이 유도되는 과정을 보여준다. |

‘표적 항암제’의 목표가 되는 암 생성ㆍ증식 생체물질을 ‘표적 인자’라고 하는데, 그 중의 대표적인 것이 ‘인슐린유사성장인자 수용체’(IGF-1R, insulin-like growth factor 1 receptor)로, 암세포의 성장, 사멸, 전이 및 항암제 내성을 매개하는 중요한 신호전달 단백질로 알려졌다. IGR-1R은 두 종류의 인슐린 유사 성장인자인 IGF1과 IGF2의 결합에 의하여 활성화되는 단백질로서 표적 항암제를 통해 억제해야 하는 표적 인자다.
연구팀에 따르면 IGF-1R의 표적 항암제가 개발돼 여러 암종을 대상으로 임상 시험이 실시돼 왔으나, 지금까지 효과를 이끌어내지 못해 암 환자의 치료에 사용되지 못했다. 연구팀은 실제로 사람 암세포를 이식한 쥐에 IGF-1R 단백질의 표적 항암제를 처리하자 이식한 종양의 성장은 억제되었으나 다른 장기로 전이암이 발생된 것을 발견했다.
이에 연구팀은 표적 항암제에 의한 종양 주변의 미세환경 세포와의 상호작용이 항암제 내성에 따른 전이암 생성을 매개한다는 가설을 수립해 연구에 착수했다.
연구팀이 동물 실험을 통해 확인한 결과, 표적 항암제에 의해 IGF-1R 단백질에 의한 신호전달이 차단됐을 때 일종의 보상 작용으로 신호전달 단백질 ‘스타트3’(STAT3)가 활성화되고, IGF2 단백질의 발현이 증가됨을 확인했다. 이렇게 생성된 IGF2 단백질은 종양 세포 주변의 세포들이 종양세포로 모여들어 상호작용을 하도록 유도했고, 모여든 세포들은 혈관내피세포의 증식을 촉진해 새로운 혈관을 생성하도록 했고 이에 따라 전이암 생성이 유발됐다는 것이 연구팀의 실험결과다.
이호영 교수팀의 연구는 IGF-1R을 목표로 한 표적항암제의 투입이 전이암으로 이어지는 원리를 최초로 규명한 것으로, 지금까지는 IGF2가 IGF1R에 결합하는 성장인자로만 인식됐으나 종용과 종용주변 미세환경 세포와의 상호작용을 매개해 암전이를 일으킨다는 사실을 밝혔다.
이호영 교수는 “암 환자의 치료 효과 감소 및 사망률 증가의 주요 원인인 항암제 내성 및 전이암 생성을 효과적으로 차단할 수 있는 신규 표적을 제시하였다는 점에서 의미가 있다”며 “특히, 항암제 처리에 의해 개체 내에서 발생될 수 있는 종양-종양 미세환경 세포와의 상호작용을 고려한 기전 연구 및 표적 발굴이라는 점에서 임상 응용성이 높을 것으로 여겨진다”고 덧붙였다.
이번 연구는 미래창조과학부의 기초연구사업(중견연구자지원사업 및 선도연구센터지원사업)으로 수행됐으며 연구결과는 자연과학 분야의 권위 있는 학술지 ‘네이처 커뮤니케이션즈’(Nature Communications) 14일자에 게재됐다.
suk@heraldcorp.com








