- 경희대 김동운 교수팀, 나노입자 활용 세포노화유도인자 억제

[헤럴드경제=구본혁 기자] 인류가 아직까지 정복하지 못한 난치성 질환 치매. 뇌 속 노화된 미세아교세포를 젊게 되돌려 뇌의 탐식 및 인지기능을 높이는 기술이 개발됐다.
미세아교세포란 뇌에서 신경 퇴행 반응을 일으키는 다양한 독성 물질을 제거하고 신경 뉴런을 보호하는 세포를 말한다.
한국연구재단은 경희대학교 김동운 교수 연구팀이 충남대학교 뇌과학연구소 신효정 박사와 공동연구를 통해 뇌세포의 80%를 차지하는 교세포 중 미세아교세포를 역노화 시키는 기술을 개발, 치매 치료 가능성을 제시했다고 밝혔다.
치매는 뇌에 독성을 띠는 아밀로이드 베타(Amyloid beta) 플라크(단백질 덩어리)가 과도하게 축적되고 그로 인해 시냅스가 사라지면서 결국 기억을 잃게 되는 병이다.
최근 연구 결과에 따르면 뇌 속 미세아교세포가 노화되면서 플라크를 먹어 치우는 탐식 기능이 저하됨에 따라 신경염증 및 뇌인지 기능 장애가 유도된다는 결과가 보고되고 있다.
하지만 미세아교세포(Microglia)의 활성을 조절할 수 있는 유전체 및 약물 전달 기술의 부재로 세포 기능 연구에 한계가 있었다.
공동연구팀은 나노입자가 미세아교세포에 높은 효율로 섭취된다는 점에 착안, 이를 통해 미세아교세포에 표적 유전체를 전달하는 방법을 고안했다.
이를 알츠하이머를 겪고 있는 동물 모델에 적용한 결과, 나노입자가 전달한 표적 유전체가 세포노화유도인자인 p16ink4a 유전자를 억제함으로써 늙은 미세아교세포를 젊은 미세아교세포로 역노화 시켰고, 이를 통해 미세아교세포의 탐식 및 인지기능이 향상된 것을 확인할 수 있었다.
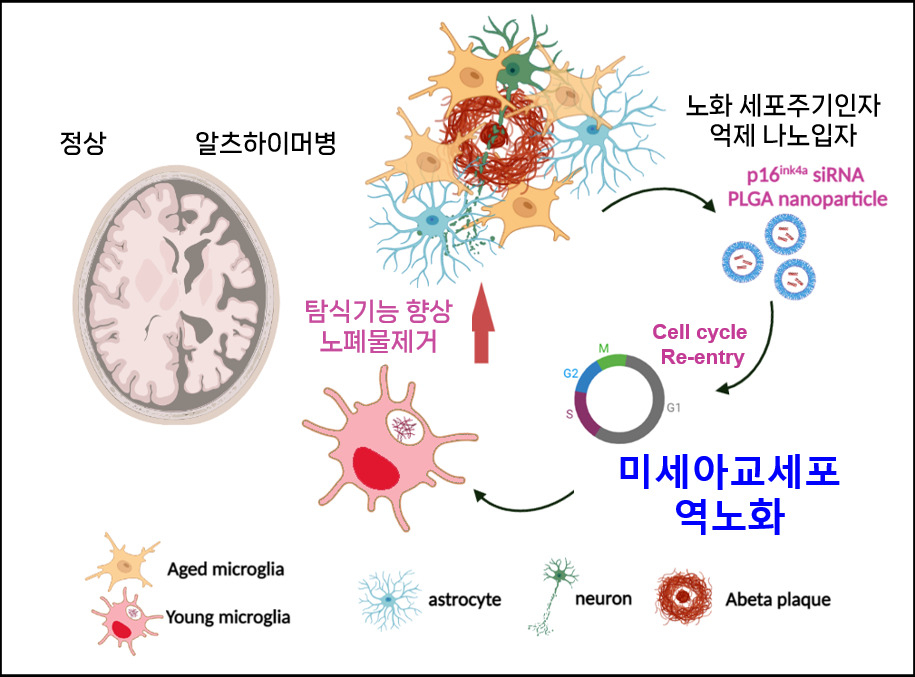
이번 연구 결과는 뇌 속 신경염증의 주요 매개체인 미세아교세포를 대상으로 역노화와 같은 기능 조절을 통해 인지력을 높일 수 있다는 가능성을 제시했다는 점에서 중요하다.
연구팀은 미세아교세포의 활성 조절을 통해 다양한 뇌질환을 극복할 수 있는 실마리를 찾을 수 있을 것으로 기대하고 있다.
김동운 교수는 “뇌 내 미세아교세포로 약물 또는 유전체 전달 조절 기술의 가능성을 제시했다는데 의의가 있다”며 “앞으로 이를 확장해 혈관뇌장벽 통과 효율을 증가시킬 수 있는 초음파활용 약물전달기술, 또는 나노입자 특성을 개선할 필요가 있다”고 말했다.
과학기술정보통신부와 한국연구재단 지원으로 수행된 이번 연구 성과는 신경과학분야 국제학술지 ‘분자 신경퇴화(Molecular Neurodegeneration)’에 3월 18일 게재됐다.






![“비트코인, 예전에 남친 말 듣고 샀는데 마이너스 77%”…사상최고 찍었는데 무슨 일? [투자360]](https://wimg.heraldcorp.com/news/cms/2024/11/22/news-p.v1.20241122.0cf61946edb24523a8f1c5a715bcae7d_T1.jpg?type=h&h=640)


![“父는 죽고, 친모와 결혼하고” 재앙같은 예언…당사자 아들의 기구한 사연[이원율의 후암동 미술관-오이디푸스 편]](https://wimg.heraldcorp.com/news/cms/2024/11/23/news-a.v1.20241122.6f410829d2e847798d1f6f02d6796a42_T1.jpg?type=h&h=240)


![집 싸게 내놔도 파리날린다…서울 아니면 공공분양도 썰렁 [부동산360]](https://wimg.heraldcorp.com/news/cms/2024/11/23/ams.V01.photo.HDN.P.20241029.202410291101280984490757_T1.jpg?type=h&h=240)




![연예인에 빠져…“24개월 할부로 사더니” 전부 쓰레기통 행 [지구, 뭐래?]](https://wimg.heraldcorp.com/news/cms/2024/11/20/news-p.v1.20241120.bf9d50d5065347f3ba37696b2898bb31_T1.jpg?type=h&h=240)
![집 너무 안팔리자 아내가 꺼낸 말 “여보, 상가랑 아파트 바꿀까?”[부동산360]](https://wimg.heraldcorp.com/news/cms/2024/11/16/rcv.YNA.20241105.PYH2024110509190001300_T1.jpg?type=h&h=240)



